イントロダクション
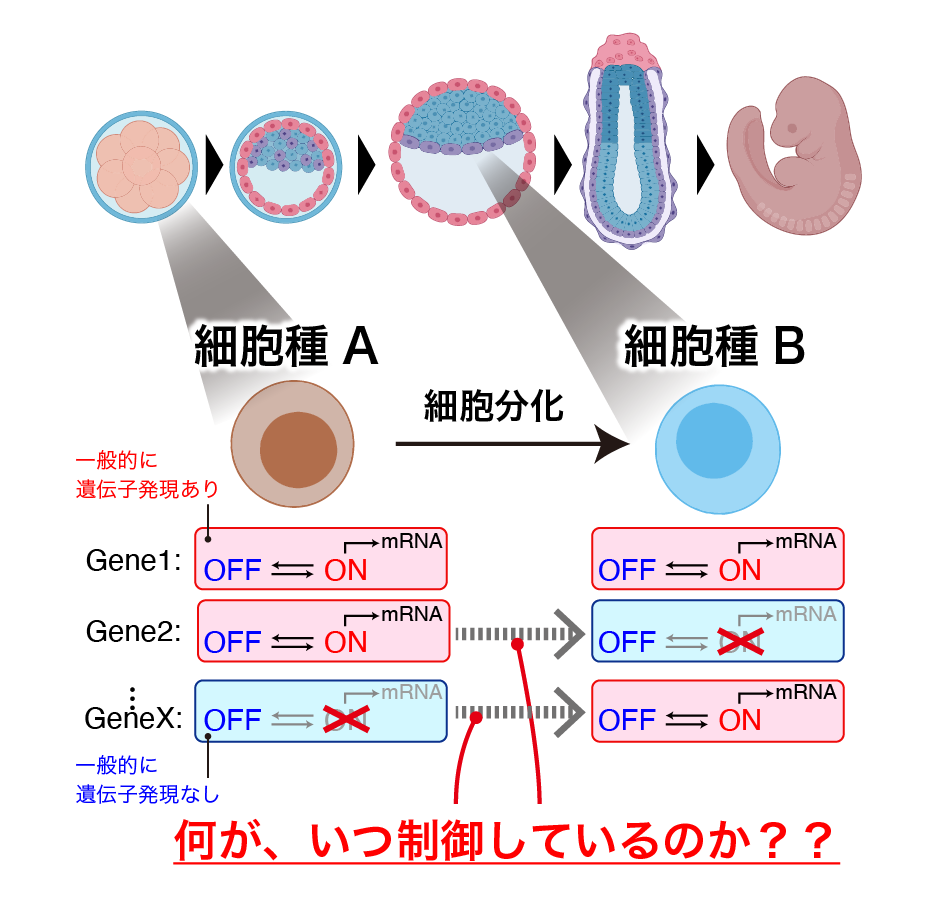
細胞運命決定とは、細胞が特定の性質や役割を獲得していくプロセスのことです。これは、未分化な細胞が特定の細胞系譜へと成熟する「細胞分化」だけでなく、細胞の生存や死(プログラム細胞死)、細胞の移動や配置の変化など、多様な現象を含む広義の概念です。同じゲノムや環境を持つ細胞集団であっても、それぞれの細胞における遺伝子発現量にはばらつき(多様性)が生じることが知られており、この一過性の遺伝子発現のゆらぎが、細胞が将来的にたどる運命に影響を与えることが示唆されています。発生過程においては、こうした遺伝子発現のゆらぎが、細胞の分化だけでなく、プログラム細胞死や細胞の移動をも決定する重要な要素となっている可能性があります。
このような遺伝子発現の多様性を生み出すメカニズムの一つに、転写バーストがあります。転写バーストとは、遺伝子の発現(転写)活動がON状態(活発にRNA合成)とOFF状態(ほとんどRNA合成しない)の間を確率的に切り替わる現象です。各遺伝子は細胞内に1〜2コピーしかないため、ON/OFFの切り替えによって生じるRNA産生のゆらぎが細胞間で大きな発現量のばらつきをもたらします(図1)。このような転写の不均一性(ノイズ)が細胞運命決定に影響を与える可能性があり、最近の研究では「確率的な転写活性が決定論的な発生過程を導く」現象として注目されています。

図1. 転写バーストとそれによって誘引される遺伝子発現量の多様性. (A)転写バーストの模式図. (B)転写バーストの有無による経時的mRNA発現量の変動. (C)転写バーストによってアレル間および細胞間で遺伝子発現量の差が生じ得る.
研究の背景
マウス初期胚の内部細胞塊は、胚盤胞期に胚内部に存在する未分化細胞の集団で、この内部細胞塊から将来的に胚体を形成するエピブラストと、胚体外組織となる原始内胚葉が分化します。内部細胞塊細胞では発生初期において、エピブラスト分化を示す転写因子NANOGと内部細胞塊分化を示す転写因子GATA6の両方をすべての細胞が共発現しています。胚の発生が進むにつれて内部細胞塊内の各細胞は次第にNANOGまたはGATA6のいずれかを高発現する状態へと分かれ(いわゆる“塩とコショウ”様のモザイクパターン形成)、最終的にNANOG陽性細胞はエピブラストに、GATA6陽性細胞は原始内胚葉へと分化します(図2)。この分化プロセスは一見ランダムに起こるように見えますが、実際にはNANOG高発現の内部細胞塊細胞は将来エピブラストになる傾向があることが示されています。また、NANOG高発現細胞から分泌されるFGF4シグナルが周囲の細胞に作用し、それらを内部細胞塊へ誘導することで最終的な細胞種の分離(ソーティング)が起こることが報告されています。このように内部細胞塊における遺伝子発現の多様性(NANOGやGATA6の発現量の細胞間差異)は、エピブラスト・原始内胚葉それぞれの細胞運命を決定づける重要な要因であると考えられています(図2)。
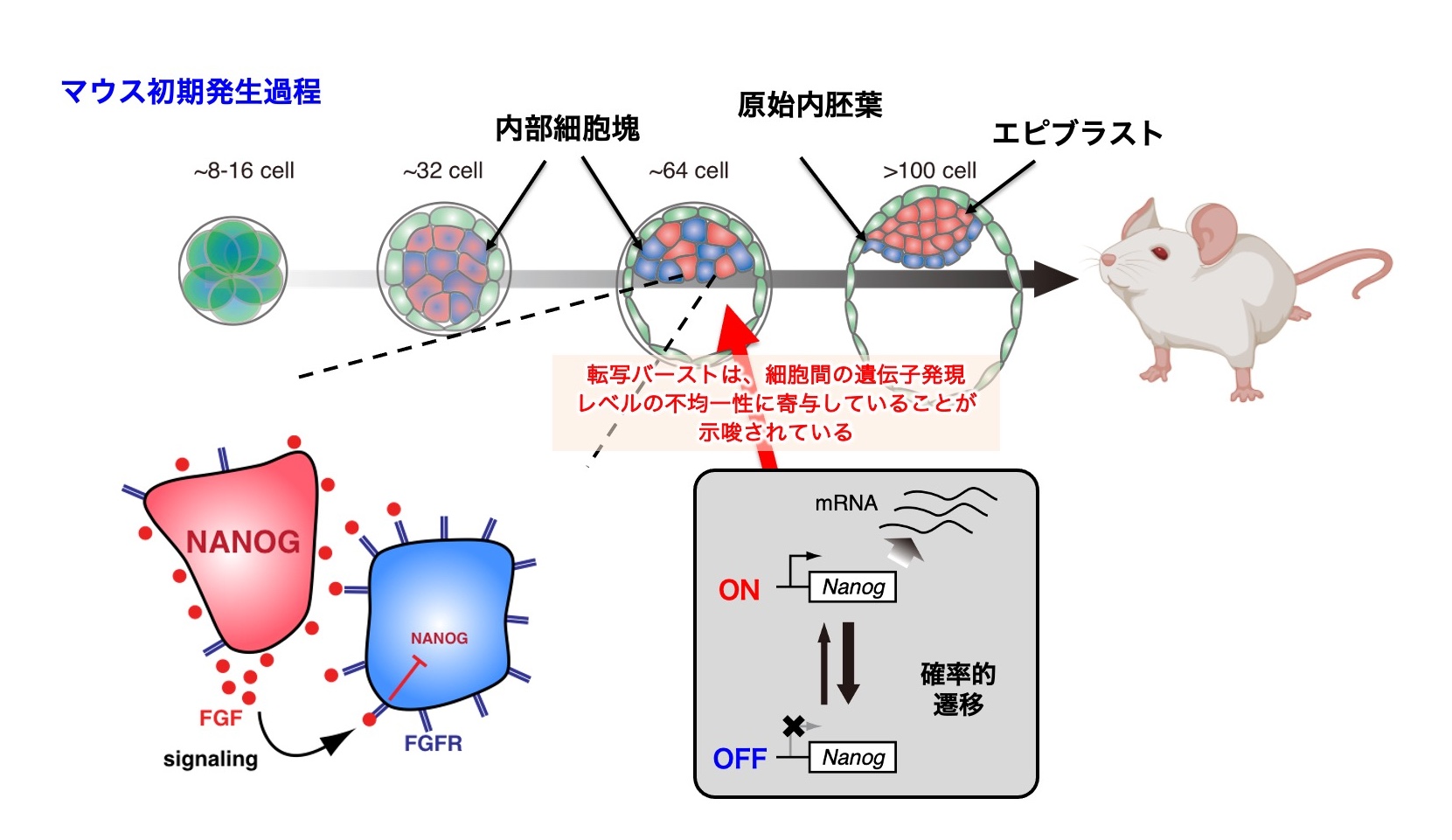
図2. マウス初期発生における遺伝子発現レベルの不均一性
しかし、内部細胞塊内部で最初にNANOGやGATA6の発現量にばらつきが生じる仕組みについては未だ明らかでない点が多く残されています。近年の研究で、Nanog遺伝子はマウス初期胚およびES細胞において一方の対立遺伝子からのみ転写される場合がしばしばあることが報告されました。これはNanog遺伝子が顕著な転写バーストを示すことを意味し、NANOG発現量の細胞間多様性(細胞ごとのNANOG量のばらつき)を生み出す一因になっている可能性があります。我々の先行研究でも、マウスES細胞において転写バースト由来のintrinsic noise(細胞内要因による発現ゆらぎ)がNanog発現量の異質性に大きく寄与することが示されました (Ochiai et al., Sci Rep, 2014; Ochiai et al., Sci Adv, 2020)。一方で、初期胚内部細胞塊において転写バーストが実際にどの程度発生し、それが細胞運命の選択にどう結びつくのかについては、直接的な検証が行われていません。内部細胞塊細胞内の転写動態を時空間的に解析し、エピブラスト・原始内胚葉への分化プロセスにおける転写バーストの役割を解明することが、本研究の背景にある未解明の課題です。
研究の目的
- 内部細胞塊における転写バーストと遺伝子発現量多様性の関係を単一細胞レベルで明らかにする。具体的には、内部細胞塊内部の各細胞で発現する重要遺伝子(例:NanogやGata6など)の転写バースト挙動を定量化し、それによって生じる細胞間の発現量ばらつきとの対応関係を解明することを目指します。
- 転写バーストがエピブラスト・原始内胚葉への分化に与える影響を解明する。すなわち、内部細胞塊細胞がエピブラストあるいは原始内胚葉へ運命決定する際に、転写バーストの頻度や強度がどのような役割を果たすのかを検証し、細胞運命決定の確率的メカニズムを明らかにします。
研究手法
DNA/RNA/IF-seqFISH
DNA-FISH、RNA-FISH、免疫染色(IF)を組み合わせた逐次的多重FISH法(seqFISH)を胚組織に適用します。これにより、内部細胞塊内の個々の細胞における複数遺伝子のmRNA発現量とタンパク質発現(転写因子の存在量)を同時に可視化・定量します。例えばNANOGやGATA6を含む発生運命決定関連因子の発現分布を一胚レベルでマッピングし、細胞間の発現多様性を高解像度で測定します。DNA-seqFISHにより各遺伝子座位でのアリルごとの転写状態も捉えることで、1細胞内の対立遺伝子別の発現(アリル発現偏り)まで解析し、転写バーストの空間分布や発現ゆらぎパターンを明らかにします。

DNA/RNA/IF-seqFISHの模式図。
seq-DNA/RNA/IF-FISHの代表的な画像。本動画は、seq-DNA/RNA-IF-FISHを用いて各ラウンドで取得された画像の最大輝度投影から作成されている。各ラウンドにおいて、3種類の二次プローブセットおよび読み取りプローブセットが使用され、3つのチャンネルを介した画像取得が可能であった。それぞれのチャンネルは単一のRNA、ゲノム領域、タンパク質、または翻訳後修飾の局在を観察するために用いられた。(Ohishi et al., Sci Adv, 2020)
生細胞単一遺伝子イメージング技術
ライブセルイメージングにより、初期胚オルガノイドにおける内部細胞塊様細胞内の特定遺伝子の転写動態をリアルタイムに観察します。具体的には、単一遺伝子可視化システム (STREAMING-tagシステム; Ohishi et al., Nat Commun, 2022) を用いてNanog等の標的遺伝子の細胞核内局在、mRNA合成イベントを可視化し、内部細胞塊様細胞での転写バーストが発生する様子を記録します。これにより転写バーストの頻度(ON状態になる頻度)やサイズ(ON一回あたり産生されるRNA数)を時間分解能高く測定し、個々の細胞がもつ転写動態の特徴を抽出しつつ、細胞運命決定との関係性を解き明かします。
単一遺伝子イメージング技術(STREAMING-tagシステム)の模式図と本技術を利用して撮影された動画。マウスES細胞のNanog遺伝子にSTREAMING-tagが適用されており、本細胞を15秒間隔で撮影した動画。
単一遺伝子イメージング技術(STREAMING-tagシステム)の模式図と本技術を利用して撮影された動画。マウスES細胞のNanog遺伝子にSTREAMING-tagが適用されており、本細胞を2分間隔で撮影した動画。
転写バーストの時空間解析
上記で得られた空間(seqFISH)および時間(ライブイメージング)の情報を総合して解析します。内部細胞塊内の位置関係と転写バースト特性の関連を調べます。また、ライブイメージングした細胞については追跡解析を行い、特定の転写バーストパターン(高頻度のバーストを示すか否か等)を示した細胞が後にエピブラストあるいは原始内胚葉へ分化する割合を解析します。これにより、転写バースト特性と細胞運命の相関を定量的に評価します。
期待される成果と意義
細胞運命決定の確率論的要因の解明
本研究により、これまでブラックボックスであった初期胚における「運命のゆらぎ」の実体(転写バーストによる遺伝子発現ノイズ)が明らかになります。発生過程に内在するランダム性と規則性の関係を定量的に示すことで、従来の決定論的な発生モデルを拡張し、細胞運命決定を支配する原理への新たな理解が得られると期待されます。特に、内部細胞塊段階での塩コショウ様の細胞分化において転写ゆらぎが果たす役割を示せれば、発生生物学における長年の疑問に答えることにつながります。
再生医療・発生生物学への応用可能性
細胞分化におけるノイズ制御機構の解明は、胚性幹細胞や誘導多能性幹細胞の分化誘導技術にもインパクトを与えます。将来的に、転写バーストの頻度や強度を人工的に操作することで、所望の細胞系譜への分化誘導効率を高めたり、分化のタイミングを制御したりできる可能性があります。また、発生過程での異常(例えば初期胚発生の失敗や流産)の原因解明にも、転写ゆらぎの観点から新たな知見を提供できるでしょう。こうした基礎知識の蓄積は、再生医療のみならず発生工学や生殖補助医療の発展にも寄与すると考えられます。
研究の将来的な展望
本研究で得られる知見は、他の細胞運命決定過程にも展開可能です。例えば、中胚葉・内胚葉の分化や体軸形成など、より後期の発生段階における細胞運命選択においても、転写バーストや遺伝子発現多様性の役割を調べることができます。また、本研究を通じて得られる転写バースト制御因子の候補は、将来的に遺伝子工学的手法で操作することで、ノイズを抑制または増幅して発生現象への影響を検証するという新たな実験系へと発展し得ます。以上のように、本研究の成果は基礎生物学的意義が高いだけでなく、将来的な応用研究への橋渡しとなる点で意義深いものです。